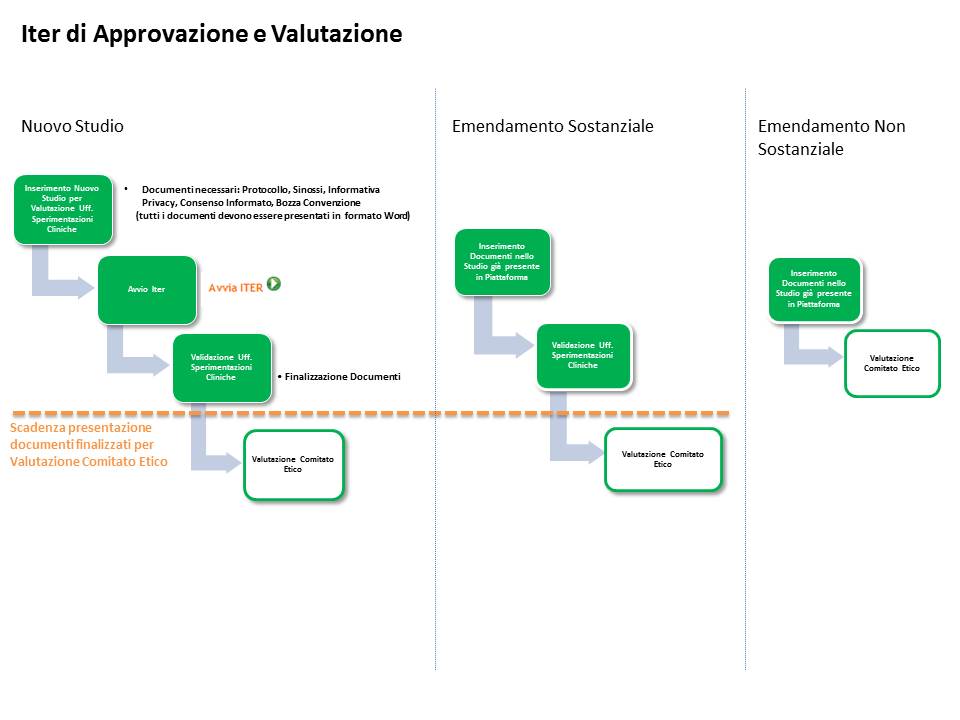
OGGETTO: Autorizzazione effettuazione sperimentazione clinica Protocollo DHEP. Allegati: 1 IL DIRETTORE GENERALE SU PROPOSTA D

Sperimentazioni cliniche, cosa prevede il nuovo regolamento europeo - I-Com, Istituto per la Competitività
OGGETTO: Nuovi Sistemi Informativi AIFA e adempimenti relativi a Sperimentazione Clinica Dal 1° gennaio 2013 l'Agenzia Italia
ART. 5 LR 33/2015 - COMITATO ETICO UNICO REGIONALE PER LA SPERIMENTAZIONE CLINICA - PROROGA. Il Direttore Centrale Decreto n° 5

Sperimentazione clinica di medicinali per uso umano: luci e ombre del nuovo Regolamento Ue - Agenda Digitale